Ariel sanchez
Consiste na hiperfunção de uma ou mais glândulas paratireoides, com aumento da concentração sérica do hormônio específico, que causa hipercalcemia. O hiperparatireoidismo primário é, junto com o câncer, uma das duas causas mais frequentes de hipercalcemia (entre as duas entidades, eles respondem por mais de 90% das elevações patológicas no cálcio sérico).
|
Figura 75-1 |
O principal agente do sistema homeostático que mantém o nível normal de cálcio no fluido extracelular é a glândula paratireoide, cuja função só começou a ser conhecida neste século. A concentração sérica fisiológica do íon cálcio é de aproximadamente 1,3 mM; sua relação com a secreção do hormônio da paratireóide (PTH) é inversa e está representada graficamente na Figura 75-1: conforme a calcemia diminui, o hormônio é liberado, que é inibido pela hipercalcemia, por exemplo, causada por uma infusão intravenosa de cálcio ou por administração oral de um composto de cálcio facilmente absorvido pelo intestino. A resposta secretora a diminuições muito pequenas no cálcio é instantânea: ocorre em segundos.
Do cálcio circulante total, metade está ligada às proteínas plasmáticas, enquanto o restante forma complexos difusíveis (citrato, etc.) ou é ionizado. O íon cálcio é essencial para a contração muscular, excitabilidade neuromuscular, permeabilidade da membrana celular e coagulação do sangue. Além disso, o cálcio é uma parte fundamental da estrutura óssea e seus níveis circulantes devem ser mantidos normais para a ossificação adequada.
O PTH atua nos osteoclastos de modo que eles reabsorvem o osso e fornecem o cálcio e o fósforo contidos na hidroxiapatita para a corrente sanguínea. Também atua no túbulo renal para aumentar a reabsorção de cálcio filtrado pelo glomérulo, para promover a excreção de fósforo, reduzindo sua reabsorção proximal e distal, e para estimular a síntese de calcitriol (1,25-dihidroxivitamina D) de seu precursor , calcidiol (25-hidroxivitamina D), por ação da enzima 1-alfa-hidroxilase. O calcitriol, por sua vez, atua no nível intestinal aumentando a absorção de cálcio e fósforo. Cada uma dessas respostas fisiológicas tende a aumentar o cálcio total (e / ou iônico) no plasma, enquanto a fosfatemia não varia ou diminui.
É bem conhecida a seqüência dos 84 aminoácidos que compõem o PTH humano, sendo que o primeiro terço - o que contém a extremidade amino - é aquele com atividade biológica; O PTH1-34 e outros fragmentos do hormônio humano já foram sintetizados.
Na glândula paratireóide, a síntese hormonal é feita a partir de um precursor, o pró-PTH, que possui 6 aminoácidos adicionais conectados à extremidade amino-terminal do PTH. O Pro-PTH é sintetizado no sistema reticuloendoplasmático rugoso das células principais e é transformado em PTH por clivagem proteolítica no aparelho de Golgi. Nas glândulas bovinas, o conteúdo de pró-PTH é de aproximadamente 10% do PTH. Não há evidências de que este precursor seja colocado em circulação. Também existe um precursor do pró-PTH, denominado pré-pró-PTH, com 115 aminoácidos (Figura 75-2).
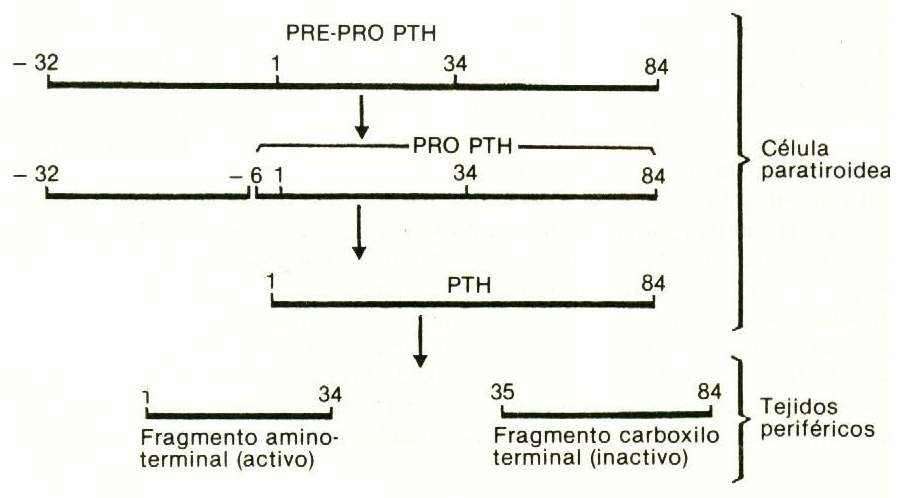 Figura 75-2 |
A hipocalcemia aumenta a conversão intracelular de pró-PTH em PTH. O PTH é armazenado em grânulos secretores; sua liberação depende de uma concentração normal de magnésio no fluido extracelular. Tanto a hiper quanto a hipomagnesemia a inibem, talvez devido a uma alteração do mecanismo de exocitose.
No sangue periférico, o hormônio intacto ou nativo e vários fragmentos são encontrados, muitos dos quais não têm atividade biológica, mas têm a identidade imunológica que os torna reconhecíveis pelos diferentes anti-soros usados para o radioimunoensaio. Essa “heterogeneidade” do hormônio circulante é uma das causas da dificuldade que às vezes se encontra na interpretação dos resultados reportados pelo laboratório. Embora parte desses fragmentos seja secretada pela própria glândula, a maioria vem do metabolismo periférico do hormônio nativo, que desaparece da circulação com meia-vida de 1 a 10 minutos; os principais locais dessa degradação do tecido são o fígado e os rins.O hormônio intacto não é capaz de mobilizar o cálcio do osso, o que, por outro lado, não o remove da circulação. Em vez de,
Como todos os hormônios peptídicos, o PTH não penetra nas células para exercer sua ação, mas se liga a receptores específicos na membrana celular, que ativam a adenil ciclase e geram adenosina monofosfato cíclico (cAMP) no citosol ("segundo mensageiro" da ação hormonal). Quando isso ocorre nas células do túbulo renal, o cAMP se difunde no lúmen tubular: seus níveis urinários aumentam rapidamente após a injeção intravenosa do hormônio; na verdade, esta é a resposta detectável mais cedo in vivo.
Fisiopatologia
No hiperparatireoidismo, os mecanismos que devem controlar a secreção normal de PTH estão prejudicados. A secreção é excessiva e autônoma, ou seja, não é retardada pela hipercalcemia que causa. Ao contrário do que ocorre em outras causas de hipercalcemia, nas quais a concentração sérica de PTH é baixa, aqui coexistem níveis elevados de cálcio e hormônio plasmático.
Basta uma das quatro glândulas (adenoma) aumentar para que o excesso de hormônio seja produzido. Essa hipertrofia uniglandular é a causa mais comum (80%) de hiperparatireoidismo primário. É seguido por hiperplasia das quatro glândulas, enquanto o carcinoma da paratireóide é raro (3% dos casos). A perda da sensibilidade normal das células da paratireóide aos níveis de cálcio livre no líquido extracelular é o principal mecanismo fisiopatológico da doença na maioria dos adenomas. Na hiperplasia difusa, o ponto de ajuste das células individuais é o normal, mas à medida que a massa das células aumenta, o excesso de hormônio é produzido. A base molecular da doença não é muito clara.
A secreção ectópica de PTH - ou seja, a produção do hormônio por tumores não paratireoides - é um fato bem estabelecido, mas relativamente incomum. Por outro lado, o pseudo-hiperparatireoidismo é muito comum, o que supõe a existência de uma substância em circulação com efeitos muito semelhantes aos do PTH. A busca por esse humor misterioso levou à descoberta do peptídeo relacionado ao PTH (PTHrP), que apresenta grande homologia ao PTH e é responsável pela grande maioria das hipercalcemia maligna.
Algumas formas de hiperparatireoidismo são hereditárias. Existem dois tipos de neoplasias ou adenomatose endócrina múltipla (MEN; síndrome de Wermer), que são detalhados na Tabela 69-1. A herança autossômica dominante parece ser demonstrada na maioria das famílias afetadas.
Tabela 75-1. Neoplasias endócrinas múltiplas
|
NÃO tipo 1 |
NÃO tipo 2 |
|
Tumores de: |
|
|
Paratireóide |
Paratireóide |
|
Hipófise |
Tireóide (carcinoma medular) |
|
Pâncreas (ilhotas) |
Medula adrenal (feocromocitoma) |
Sintomas e sinais
 Manifestações osteoarticulares . Eles estão presentes em metade dos pacientes afetados. Geralmente, há dor óssea vaga ou localizada e artralgia. A artrite aguda pode ocorrer devido à deposição de cristais de pirofosfato de cálcio bidratado nos meniscos e cartilagens articulares (pseudogota devido à condrocalcinose) ou de cristais de urato monossódico (gota), com hiperuricemia e hiperuricosúria freqüentes no hiperparatireoidismo.
Manifestações osteoarticulares . Eles estão presentes em metade dos pacientes afetados. Geralmente, há dor óssea vaga ou localizada e artralgia. A artrite aguda pode ocorrer devido à deposição de cristais de pirofosfato de cálcio bidratado nos meniscos e cartilagens articulares (pseudogota devido à condrocalcinose) ou de cristais de urato monossódico (gota), com hiperuricemia e hiperuricosúria freqüentes no hiperparatireoidismo.
A radiologia pode mostrar osteopenia difusa (este é o achado mais comum), esmagamento vertebral, cistos ósseos nos ossos longos (Fig. 76-3) e reabsorção subperiosteal no aspecto radial das primeiras falanges dos dedos (Fig. 76- 3). 76-4). Às vezes, a calota craniana tem uma aparência pontilhada ("sal e pimenta") que não é patognomônica. A lâmina dura dos alvéolos dentais pode ser fina ou ausente. A calcificação das cartilagens articulares, sinal típico da condrocalcinose, só pode ser demonstrada radiograficamente; também pode haver calcificações periarticulares.
Manifestações renais . 55% dos pacientes apresentam nefrolitíase, de modo que os sintomas e sinais clássicos dessa entidade e suas complicações (cólica renal, hematúria, infecção urinária) costumam ser a primeira forma de apresentação dessa endocrinopatia. As pedras são geralmente feitas de fosfato de cálcio ou oxalato e opacas aos raios-X.
A função renal pode estar normal ou diminuída. As doenças tubulares são comuns: perda urinária de bicarbonato, com acidose sistêmica hiperclorêmica; diminuição da capacidade de concentração urinária, com poliúria; glicosúria renal, aminoacidúria, etc. A pielografia intravenosa ajuda a avaliar a árvore urinária e também permite descobrir, quando existem, calcificações do parênquima renal (nefrocalcinose). A ultrassonografia renal é um método não invasivo e útil para avaliar a possibilidade de cálculos.
Manifestações musculares . Fraqueza muscular e fadiga fácil são sintomas comuns. O primeiro é mais perceptível na musculatura proximal dos membros: os pacientes têm dificuldade em tirar a camisa, ficar de pé ou subir escadas; pode haver atrofia muscular. A velocidade de condução nervosa é normal, mas a eletromiografia e a biópsia muscular mostram alterações compatíveis com desnervação, sem alterações inflamatórias. As enzimas séricas (transaminase glutâmica oxaloacética, creatina fosfoquinase e aldolase) são sempre normais. Portanto, não é uma miopatia, mas sim uma neuropatia.
Manifestações gastrointestinais . A úlcera péptica é muito comum (mais de 20% dos casos). A hipercalcemia produz hipergastrinemia e isso leva ao aumento da secreção de ácido no estômago. Não se deve perder de vista a possível associação de um adenoma de paratireoide com um gastrinoma (síndrome de Zollinger-Ellison) ou com hiperplasia difusa das ilhotas pancreáticas, como parte de um MEN tipo 1. Deve-se lembrar, entretanto, que esses casos representam uma parcela muito pequena dos pacientes com a combinação de hiperparatireoidismo primário e úlcera. A pancreatite, especialmente a forma dolorosa crônica, pode ser uma complicação digestiva do hipoparatireoidismo. Já se sabe que a pancreatite aguda produz diminuição do cálcio total; portanto,
Outras manifestações . Sede, poliúria, constipação, anorexia e desconforto abdominal. É comum observar transtornos mentais, com alterações de personalidade, depressão e até psicose.
A hipertensão geralmente está associada, embora isso provavelmente se deva à alta prevalência desse distúrbio na população em geral. A anemia deve ser adicionada à lista de complicações. É moderada, normocrômica, normocítica e sem aumento dos reticulócitos (anemia hiporregenerativa). Podem ser encontradas calcificações em tecidos moles como córnea (ceratopatia em banda) e pele, com necrose cutânea.
Metodologia de estudo
Embora o clínico deva suspeitar de hiperparatireoidismo primário para qualquer um dos sintomas e sinais mencionados acima, deve-se enfatizar que a maioria dos pacientes é assintomática e que apenas a demonstração de sua hipercalcemia poderia detectá-los. A hipercalcemia é o único sinal invariável e onipresente no variado quadro clínico dessa doença. Sem ele, documentado em mais de uma ocasião por um laboratório de contabilidade, não se justifica submeter o paciente a outros estudos mais caros e demorados. O intervalo normal para o cálcio é de 8,5 a 10,6 mg / dl. Sua interpretação requer que seja conhecida a concentração sérica de proteínas, uma vez que a hiperproteinemia pode causar aumento dos níveis de cálcio total, a hipoproteinemia pode mascarar a hipercalcemia.Deve-se enfatizar a importância de várias dosagens do cálcio, uma vez que sua elevação pode ser sustentada ou intermitente. Este último ocorre em casos leves, com valores de calcemia no limite superior da faixa normal, ou apenas ligeiramente elevados (hiperparatireoidismo “normocalcêmico”).
O cálcio iônico plasmático quase sempre está elevado. Sua medição requer um aparato especial, equipado com um eletrodo de fluxo sensível a íons.
Outros sinais que devem ser procurados para confirmar o diagnóstico são:
- PTH circulante aumentado (a documentação simultânea de hipercalcemia e nível de PTH elevado demonstra o colapso do sistema homeostático representado na Figura 69-I); na presença de hipercalcemia, os níveis de PTH na faixa normal alta são consistentes com o diagnóstico. A maioria dos equipamentos comerciais disponíveis hoje mede o hormônio "intacto" ou "inteiro" (todos os 84 aminoácidos) por técnica imunorradiométrica (IRMA).
- hipercalciúria (> 400 mg / dia);
- hipofosfatemia (pode estar ausente em pacientes com algum grau de insuficiência renal);
- a diminuição da reabsorção tubular de fósforo (seu valor normal deve ultrapassar 85%);
- o aumento da fosfatase alcalina –especialmente de sua isoenzima óssea–, que reflete o maior número e intensa atividade dos osteoblastos, empenhados na reparação do osso reabsorvido pelos osteoclastos; está muito aumentado nos casos de osteíte fibrosa cística; também aumenta a osteocalcina sérica, outro marcador bioquímico da função osteoblástica;
- o aumento em marcadores bioquímicos de reabsorção óssea (hidroxiprolina urinária, ligações de piridínio, peptídeos terminais de procolágeno tipo III, etc.);
- o aumento da cMA urinária, que denota estimulação tubular excessiva pelo PTH.
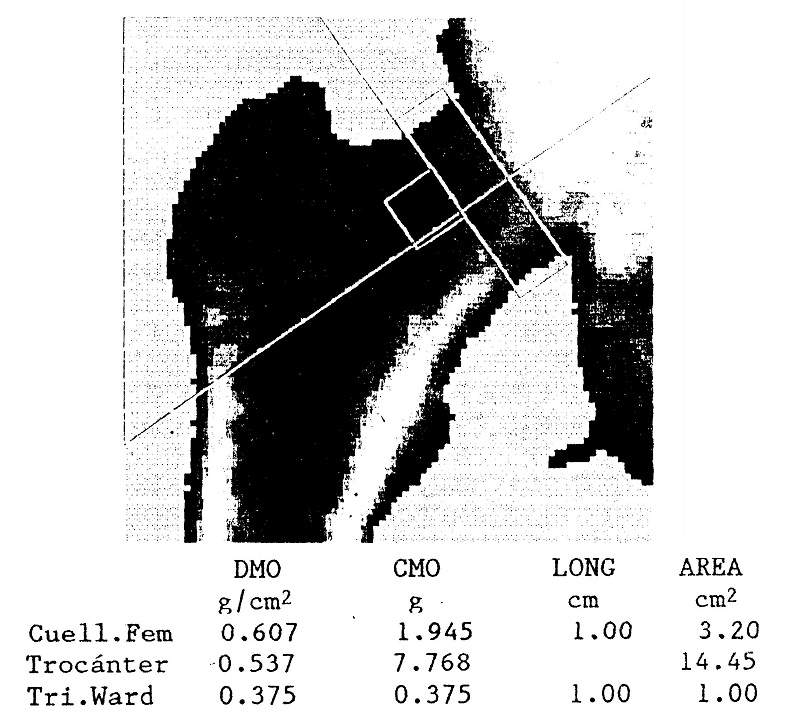
A densitometria é muito mais precisa e confiável do que a radiografia simples na detecção de diminuições no conteúdo mineral ósseo. Como o hiperparatireoidismo primário afeta preferencialmente o osso cortical, a avaliação densitométrica dos locais ósseos com abundância desse tipo de osso, como a diáfise radial ou o colo do fêmur, deve ser preferida.
É aconselhável investigar o cálcio em todos os pacientes que consultam para:
- úlcera péptica ou pancreatite;
- dor crônica nos ossos e nas articulações de origem incerta; osteopenia radiológica; fraturas vertebrais; condrocalcinose;
- nefrolitíase de cálcio, especialmente se for recorrente;
- quadros psiquiátricos mal definidos, com alterações de personalidade e depressão;
- fraqueza muscular proximal nos membros;
- qualquer combinação das manifestações acima;
- neoplasias de qualquer origem, com ou sem metástases ósseas.