Ariel sanchez
A) A osteoporose é definida como um distúrbio esquelético caracterizado por menor resistência óssea, que predispõe a fraturas. A resistência óssea reflete a integração de 2 características principais: densidade e qualidade óssea. A densidade óssea é expressa em gramas de mineral por área ou por volume e, em qualquer indivíduo, é determinada pelo pico de massa óssea alcançado e pela quantidade de osso perdido posteriormente. A qualidade se refere à arquitetura, substituição, acúmulo de danos (por exemplo, microfraturas) e mineralização. Uma fratura ocorre quando uma força (trauma) é aplicada a um osso osteoporótico. É por isso que a osteoporose é um importante fator de risco para fraturas, e uma distinção deve ser feita entre os fatores de risco para osteoporose e os fatores de risco para fraturas.
B) É importante corrigir o equívoco comum de que a osteoporose sempre vem da perda óssea. A perda de tecido ósseo geralmente ocorre com a idade dos homens e mulheres; no entanto, um sujeito que não atinge a massa óssea ideal durante a infância e adolescência pode desenvolver osteoporose sem perda óssea acelerada. Portanto, um desenvolvimento ósseo subótimo durante o crescimento é tão importante quanto a perda óssea na gênese da osteoporose.
C) No momento não existe uma medida exata da resistência óssea em geral. A densidade mineral óssea (DMO) é frequentemente usada como medida substituta, uma vez que explica aproximadamente 70% da resistência óssea. A Organização Mundial da Saúde (OMS) dá uma definição operacional de osteoporose como “uma DMO de 2,5 desvios-padrão (DP) abaixo da média de mulheres brancas, adultos jovens” (20-30 anos). Não está claro como esse critério diagnóstico se aplica a homens, meninos e outros grupos étnicos.Devido à dificuldade de obter medidas exatas e uma padronização entre diferentes instrumentos (chamados densitômetros) e diferentes locais de medidas anatômicas (coluna vertebral, quadril, antebraço distal, falanges ou metacarpos, tíbia, calcâneo, etc.), existem controvérsias entre os especialistas a respeito a validade deste critério diagnóstico.
D) A osteoporose pode ser classificada em primária ou secundária. A primária pode ocorrer em ambos os sexos em qualquer idade, mas geralmente ocorre após a menopausa nas mulheres e, posteriormente, nos homens também. Secundário é o resultado de medicamentos ou outras doenças (por exemplo, osteoporose induzida por glicocorticóides, hipogonadismo ou doença celíaca).
E) Fraturas osteoporóticas características são aquelas que seguem impactos de energia relativamente baixa (curvar-se, levantar um objeto pesado, cair de uma altura baixa, etc.). A incidência de fraturas é alta em pessoas com osteoporose e aumenta com a idade. A probabilidade de uma pessoa caucasiana de 50 anos sofrer uma fratura de quadril pelo resto da vida é de 14% para uma mulher e de 5 a 6% para um homem. Há estudos abundantes mostrando que indivíduos que sofrem fraturas de qualquer tipo, independentemente da idade e do sexo, têm menos DMO do que controles saudáveis. Portanto, uma história de fratura deve levantar a suspeita de osteoporose.
Fisiopatologia
A perda progressiva de massa óssea após os 40 anos é um fenômeno quase fisiológico, que ocorre em ambos os sexos, em todas as latitudes e em todas as raças, embora seja menos frequente na raça negra. Há 30% menos massa óssea em idosos (70-80 anos) do que em jovens (20-30 anos), sendo o conteúdo de cálcio do esqueleto menor nos primeiros.
O processo pode afetar preferencialmente o osso trabecular ou osso compacto, que se torna mais "poroso". No osso osteoporosisco, a relação entre a matriz mineralizada e a matriz não mineralizada é normal. Em outras palavras, embora o volume do osso diminua, o osso que permanece está adequadamente calcificado.
Existem três populações de células bem definidas no tecido ósseo: osteoblastos, envolvidos na aposição de novo osso; osteoclastos, especializados em reabsorção óssea; e os osteócitos, células maduras que perderam a capacidade de sintetizar osso e são capazes, em circunstâncias especiais, de reabsorvê-lo. A formação e a reabsorção óssea são processos contínuos ao longo da vida, no que é conhecido como remodelação. Isso ocorre em todas as superfícies do osso: endosteal, periosteal e intracortical ou haversiana. Em geral, existe uma estreita relação entre formação e reabsorção. A presença e o tipo de atividade nas superfícies ósseas podem ser demonstrados por várias técnicas, incluindo avaliação quantitativa das classes de células em seções finas não desmineralizadas,
O equilíbrio entre ganho e perda óssea é provavelmente devido à atividade coordenada de "feixes" de células em interação em um volume relativamente pequeno de osso; Isso é o que Frost chamou de "unidades multicelulares básicas".
A maioria das superfícies ósseas são geralmente inativas. Dados morfométricos obtidos a partir de biópsias da crista ilíaca em adultos normais indicam que a superfície de neoformação (coberta com osteóide, ou seja, osso novo ainda não calcificado) é de 10% da superfície total, enquanto a superfície da mola representa apenas 2-4% da superfície total. Estudos cinéticos com Ca47 indicam que o pool de cálcio (cálcio no fluido extracelular e tecidos moles e cálcio intercambiável no osso) é de aproximadamente 5 g. Em adultos normais, 0,5 g de cálcio entra e sai do osso todos os dias. Pode-se calcular que 1/6 do esqueleto é reabsorvido anualmente, para ser substituído novamente.
Mineralização é o processo pelo qual o mineral inorgânico é depositado na matriz orgânica. Como o mineral é composto de cálcio e fósforo, a concentração desses íons no plasma e no fluido extracelular influencia sua formação. Osteoblastos e osteócitos podem ser capazes de regular a concentração local de cálcio e fósforo e outros fatores importantes, como magnésio e pH. O colágeno pode catalisar a nucleação da fase mineral a partir de soluções contendo Ca e P. No entanto, acredita-se que existam inibidores capazes de regular a mineralização in situ. O pirofosfato inorgânico é um potente inibidor da calcificação. A fosfatase alcalina, presente nos osteoblastos, pode catalisar a hidrólise do pirofosfato,e talvez essa enzima tenha um papel na regulação do depósito de sais minerais. O mineral recém-depositado é amorfo e sua razão molar Ca / P é relativamente baixa. À medida que amadurece, se transforma em hidroxiapatita cristalina. Quando as concentrações de cálcio e fósforo estão altas no fluido extracelular, o mineral pode ser depositado em tecidos que geralmente não calcificam; pelo contrário, se suas concentrações são baixas, o mineral ósseo não pode se formar bem.
O processo de reabsorção não está suficientemente esclarecido, principalmente no que diz respeito à remoção dos íons da matriz. Este é dissolvido pelas colagenases, mas tais enzimas não podem degradar a proteína antes que ela seja desprovida da fase mineral.
Vários hormônios têm efeitos profundos no crescimento e na remodelação óssea. O hormônio paratireóideo (PTH) tem influências quase imediatas nas células ósseas, como influxo de cálcio nas células ósseas, ativação da adenil ciclase com produção intracelular de monofosfato de adenosina cíclica e captação de uridina e vários aminoácidos. Os osteoclastos são os alvos preferenciais para a ação desse hormônio, mas seus efeitos crônicos envolvem, além de estimular os osteoclastos pré-existentes, a formação de novos. O PTH também atua diretamente sobre os osteoblastos, que possuem receptores específicos. Grande parte do efeito do PTH sobre os osteoclastos é mediado por osteoblastos, que secretam, sob a influência do PTH, citocinas com efeito nessas células.
Os metabólitos ativos da vitamina D, notadamente 1,25-diidroxicolecalciferol ou calcitriol, também são capazes de aumentar a atividade e o número de osteoclastos; sua ação de mola é sinérgica com a do hormônio da paratireóide.
A ação hipocalcêmica da calcitonina foi conhecida logo após sua descoberta e parece ser devida aos efeitos diretos de parada sobre os osteoclastos. A inibição da reabsorção óssea tem início rápido, mas desaparece assim que o hormônio é removido. Após a administração de calcitonina, foram observados níveis aumentados de hormônio da paratireóide, provavelmente estimulados pela diminuição do cálcio plasmático.
Os osteoblastos e os osteoclastos requerem a presença de tiroxina para sua função normal. A hipertiroxinemia aumenta tanto a formação quanto a reabsorção, preferencialmente a última.
Os glicocorticóides inibem a transformação das células precursoras em osteoclastos in vitro, diminuindo assim a resposta de reabsorção do osso ao hormônio da paratireóide. In vivo, o excesso desses esteroides estimula a reabsorção óssea, embora possa ser um efeito indireto: ao diminuir a absorção intestinal de cálcio por um lado e aumentar a calciúria por outro, eles induzem um balanço negativo de cálcio que pode levar ao hiperparatireoidismo secundário. Por outro lado, os glicocorticóides inibem a expressão de muitos fatores de crescimento com efeito anabólico nos osteoblastos; portanto, na osteoporose metacorticóide, a função osteoblástica está muito diminuída; os corticosteróides retardam o fechamento das fraturas.
| Tabela 78-1. Fatores de controle humoral de osteoblastos e osteoclastos | ||
|
Osteoblastos |
Osteoclastos |
|
|
Estimular |
Tensão mecânica, calcitriol, esteróides sexuais, somatotropina, fator de crescimento semelhante à insulina 1, PTH |
Tiroxina, PTH, calcitriol, prostaglandinas, fator de necrose tumoral alfa, outras citocinas |
|
Inibir |
Imobilização, velhice, glicocorticóides |
Calcitonina, estrogênios, bisfosfonatos |
Um sistema de sinalização entre as células ósseas é conhecido há relativamente pouco tempo: existe um fator na membrana das células da linhagem osteoblástica que é induzido por fatores que estimulam a reabsorção (por exemplo, PTH). Esse ligante, membro da superfamília do fator de necrose tumoral (TNF), é denominado RANKL (ligante do receptor ativador do fator nuclear kappa). Ele se liga a um receptor altamente específico, RANK, uma proteína transmembrana expressa pelos osteoclastos. A ligação desse receptor ao seu ligante induz uma cascata de eventos intracelulares que levam à diferenciação das células precursoras em osteoclastos e à ativação de osteoclastos maduros. Além disso, os osteoblastos secretam um pró-peptídeo de 401 aminoácidos que, quando dimerizado, torna-se ativado e pode atuar como um receptor "chamariz";é conhecido como osteoprotegerina (OPG). É um receptor solúvel, não ligado à membrana celular e que se interpõe entre RANK e RANKL, impedindo a interação entre eles e, portanto, inibindo a ativação dos osteoclastos. Ou seja, para se diferenciar e amadurecer, as células da linhagem osteoclástica devem ter contato direto com os osteoblastos. Quanto mais RANKL e menos OPG houver em um determinado microambiente, maior será o número e a atividade dos osteoclastos; Por outro lado, quanto menos RANKL e mais OPG estiverem presentes, menos osteoclastos ativos (ver Fig. 79-1). para se diferenciar e amadurecer, as células da linhagem osteoclástica devem ter contato direto com os osteoblastos.Quanto mais RANKL e menos OPG houver em um determinado microambiente, maior será o número e a atividade dos osteoclastos; Por outro lado, quanto menos RANKL e mais OPG estiverem presentes, menos osteoclastos ativos (ver Fig. 79-1). para se diferenciar e amadurecer, as células da linhagem osteoclástica devem ter contato direto com os osteoblastos. Quanto mais RANKL e menos OPG houver em um determinado microambiente, maior será o número e a atividade dos osteoclastos; Por outro lado, quanto menos RANKL e mais OPG estiverem presentes, menos osteoclastos ativos (ver Fig. 79-1).
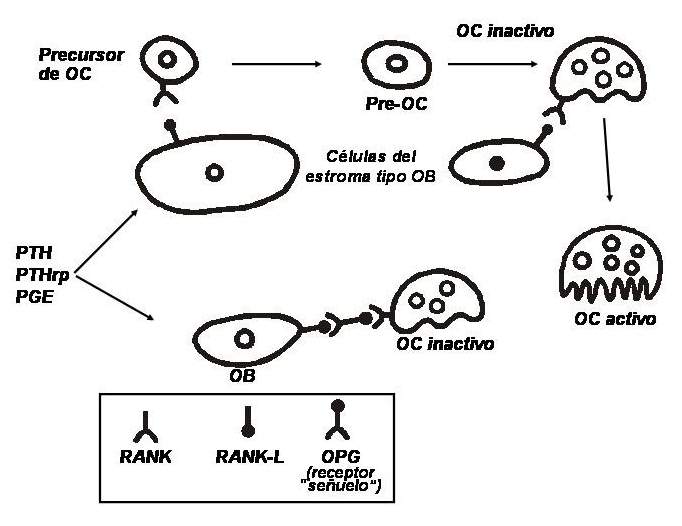
Sistema de regulação entre osteoblastos e osteoclastos. (Abreviações: OB, osteoblasto; OC, osteoclastos; OPG, osteoprotegerina; RANK, receptor ativador do fator nuclear kappa; RANKL, ligante RANK; PTH, hormônio da paratireóide; PTHrp, peptídeo relacionado ao PTH; PGE, prostaglandina E).
Os hormônios sexuais têm um papel fisiológico no controle da reabsorção. In vivo, a administração de estrogênios ou androgênios reduz a reabsorção óssea e favorece um balanço positivo de cálcio, pelo menos em curto prazo. Foi postulado que os estrogênios tornam os osteoclastos mais refratários à ação do hormônio da paratireóide. Existem receptores de estrogênio nas células ósseas da linha de osteoblastos.
Considerando os principais fatores que regulam a dinâmica da remodelação, um fato parece incontestável: para que ocorra a osteoporose, a reabsorção óssea deve ultrapassar a formação. Isso pode acontecer em qualquer uma das seguintes situações:
a) a formação diminui enquanto a reabsorção continua em sua taxa normal;
b) a formação continua normalmente, mas a reabsorção é acelerada.
Diferentes técnicas forneceram argumentos para as duas hipóteses, mas é mais provável que uma perda anual de massa esquelética maior que 1%, capaz de produzir manifestações clínicas, seja devida a uma combinação de mecanismos:
e) diminui a formação óssea e aumenta a reabsorção.
A Tabela 78-2 fornece uma classificação das diferentes osteoporose de acordo com sua causa. Se um processo de doença for identificado ao qual a osteopenia pode ser atribuída (por exemplo, hiperparatireoidismo ou hipercortisolismo), ele é considerado “secundário”. Do contrário, conclui-se que se trata de uma osteoporose “primária” ou “idiopática”, da qual se reconhece um tipo juvenil muito raro, que afeta principalmente homens entre 20 e 40 anos, sendo a forma mais comum, a Involução ou a osteoporose senil, que afeta predominantemente mulheres a partir dos 50 anos, também recebe o adjetivo "pós-menopausa".
Tabela 78-2
A fisiopatologia deste último é a mais bem estudada e está resumida na Figura 79-2.
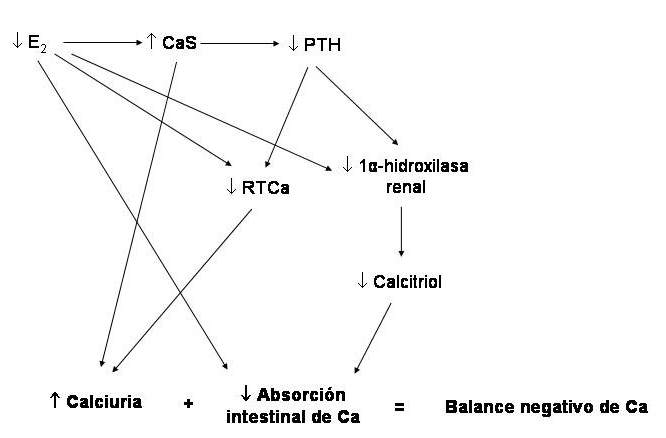
Figura 78-2: Fisiopatologia da osteoporose pós-menopausa. (Abreviaturas: E2, estradiol; PTH, hormônio da paratireóide; RTCa, reabsorção tubular de cálcio).
Ao diminuir o conteúdo de estrogênio devido à cessação da função ovariana (castração, menopausa), ocorre desrepressão da síntese de inúmeras citocinas de origem linfo e monocítica (as principais são as interleucinas 1 e 6, e o fator de necrose tumoral alfa), que ativam os osteoclastos e, portanto, causam maior atividade da mola, com leve aumento dos níveis de cálcio, o que retarda a secreção de PTH. As consequências são um aumento da reabsorção tubular de fósforo e uma diminuição da de cálcio. Há um aumento do fósforo sérico e do cálcio urinário; a hipercalciúria é acentuada pela falta de estimulação da reabsorção tubular de cálcio normalmente exercida pelos estrogênios.Tanto a diminuição do PTH circulante quanto o aumento da fosfatemia inibem a atividade da 1-alfa-hidroxilase renal, com menor produção de calcitriol e, consequentemente, menor absorção intestinal de cálcio. Além disso, diminui devido à falta de estimulação direta de estrogênios. O balanço de cálcio tende a ser negativo. Com pequenos saldos negativos, nada acontece no curto prazo, mas se a situação persistir por meses e anos, o depósito do qual foi extraído o cálcio - o osso - sofrerá o impacto da perda cumulativa (exemplo: -20 mg / dia durante 3 anos = -2,2 kg de cálcio).Outro aspecto importante do espectro fisiopatológico dessa doença é a apoptose (morte celular programada) sofrida pelos osteoblastos e osteócitos devido à falta de estrogênios e ao aumento das citocinas citadas acima. Com isso, a formação óssea diminui e o processo de reparo de microdanos no tecido ósseo torna-se menos eficiente.
A fisiopatologia da osteoporose senil é um pouco diferente: nos idosos, a menor geração de vitamina D na pele devido ao efeito dos raios ultravioleta do sol, a diminuição da síntese de calcitriol pelos rins e a menor eficácia da absorção intestinal de cálcio, com menor capacidade de adaptação a dietas com restrição de cálcio. Isso leva ao hiperparatireoidismo secundário, que acelera a renovação óssea. O déficit relativo do hormônio do crescimento em idosos e a geração local e sistêmica mais baixa do fator de crescimento semelhante à insulina 1 (IGF-1) provavelmente também desempenham um papel.
|
Tabela 78-3. Causas da osteoporose
|
Sintomas e sinais
Na síndrome osteopênica, os sintomas são geralmente vagos e inespecíficos, e não há sinais "patognomônicos".
Geralmente, o paciente queixa-se de dor difusa e mal definida nos ossos ou nas articulações, que geralmente está localizada na coluna vertebral. Quando ocorre uma fratura vertebral (esmagamento) - com ou sem desencadear estresse ou trauma - a dor é intensa e localizada, podendo irradiar-se para a parte anterior do tórax ou abdômen, dependendo da altura da vértebra afetada. Pode haver dor lombar crônica leve ou moderada.
Em sujeitos que sofreram colapso de mais de uma vértebra, há diminuição da altura, que é menor que a envergadura (distância que separa as pontas dos dedos maiores de ambas as mãos, com os braços estendidos em cruz). Há uma diminuição da distância vértice-púbis em relação ao púbis-sola, que normalmente são iguais. O ponto inferior da crista costal se aproxima da asa ilíaca e pode tocá-la; além disso, os braços em repouso parecem mais longos, com as mãos mais próximas dos joelhos (Fig. 78-3).
Quando duas ou mais vértebras dorsais consecutivas são esmagadas, a angulação da coluna leva a um exagero da cifose dorsal fisiológica, com o aparecimento de uma protuberância. Além disso, há uma deformidade de toda a caixa torácica e um exagero compensatório da lordose cervical.
Embora as fraturas vertebrais, como as do colo femoral, sejam vistas com mais frequência em pacientes idosas, nas mulheres e durante os primeiros anos após a menopausa é mais comum ver as fraturas do punho (terço distal do rádio e ulna).
Exceto no caso de fraturas recentes, não há dor com a pressão dos ossos pelo observador. Caso contrário, os pacientes com osteoporose primária estão em bom estado geral. Em contraste, aqueles com osteoporose secundária geralmente apresentam os sintomas e sinais de doenças associadas.
F) Em mulheres na pré-menopausa com osteoporose, acredita-se que 1 em cada 2 tenha uma forma secundária desta doença, sendo as causas mais comuns hipoestrogenismo, corticosteroides, excesso de hormônio tireoidiano (endógeno ou exógeno) e terapia anticonvulsivante. Em mulheres na pós-menopausa, a prevalência de causas secundárias é certamente muito menor, mas a proporção real não é conhecida. Hipercalciúria, hiperparatireoidismo e má absorção são causas a serem levadas em consideração e fáceis de confirmar ou descartar (solicitação de calcemia, calciúria de 24 horas, estudo de digestibilidade das fezes, anticorpos antigliadina e antiendomísio, por exemplo). Em outras palavras, estudos complementares em mulheres pós-menopáusicas com osteoporose podem ser necessários em casos individuais,
Metodologia de estudo
Uma boa história médica e um exame físico completo são essenciais na avaliação do risco de fratura, e a medida da altura deve ser incluída: perdas de altura> 3 cm são indicativas de esmagamento vertebral, assim como a cifose dorsal.
A radiologia permite uma avaliação, ainda que grosseira, da magnitude do processo, o que provoca um aumento da transparência dos ossos. Para quantificar com mais precisão, diferentes métodos são usados. Um deles, avaliando osso esponjoso, requer radiografias de ambas as cabeças femorais para comparar o grau de “não trabeculação” com um padrão (índice de Singh; Fig. 78-4). Outro, útil para avaliar osso compacto, estabelece a relação corticomedular em ossos longos; O segundo metacarpo da mão não dominante é geralmente usado (radiogrametria de Garn). Normalmente, a soma das espessuras de ambos os córtices deve ser maior ou igual ao diâmetro do canal medular;conforme o osso compacto é perdido, o córtex diafisário se torna mais fino e o diâmetro do canal medular aumenta.
As vértebras dorsais, ao cederem a sua estrutura face às forças compressivas, assumem - quando vistas de perfil - a forma de cunha; a lombar, devido à protrusão generalizada dos discos intervertebrais, assume uma forma bicôncava, como vértebras de peixe (Figs. 72-5 e 72-6).
Outros métodos muito mais exatos, precisos e não invasivos permitem estimar o conteúdo mineral ósseo: a densitometria radiológica e a tomografia axial computadorizada quantitativa medem a atenuação de um único ou duplo feixe de fótons que passa pelo corpo. Isso permite a determinação do conteúdo de cálcio na coluna lombar, no fêmur proximal ou em outras regiões (Fig. 78-7).
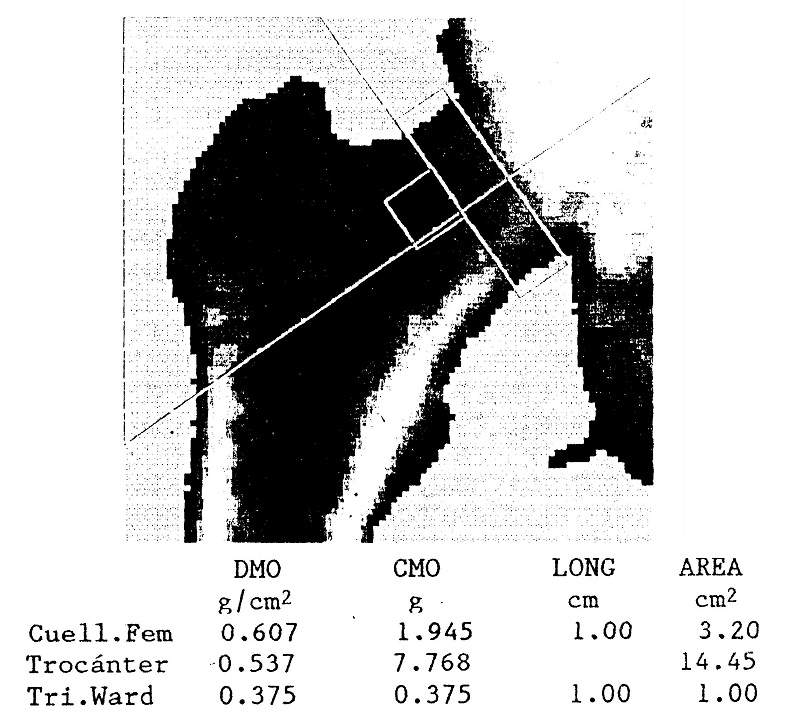
Figura 78-7: Imagem densitométrica da extremidade proximal de um fêmur direito, estudada por absortometria de raio-X duplo. O conteúdo mineral ósseo (CMO, em gramas), a área (em cm2) e a densidade mineral óssea (DMO) são relatados, em g / cm2) do colo femoral, trocanter maior e triângulo de Ward.
O ultrassom também é usado para avaliar a qualidade do osso periférico (o local geralmente estudado é o calcâneo). A densitometria se correlaciona fortemente com a resistência à fratura de quadril e vértebras em testes biomecânicos, e também prediz com precisão o risco de fratura. Diferentes locais do esqueleto e conteúdo mineral do esqueleto total podem ser avaliados, embora a densitometria de corpo inteiro seja reservada para casos especiais e investigações clínicas.
Para o diagnóstico, utiliza-se o critério de um comitê de especialistas da OMS, que utiliza o valor T (definido como o número de DPs acima ou abaixo da média correspondente a mulheres jovens saudáveis). O valor T deve ser diferenciado do Z, que é definido como o número de DPs acima ou abaixo da média correspondente a sujeitos da mesma idade e do mesmo sexo. De acordo com a definição da OMS, a osteoporose está presente quando o valor T é inferior a -2,5 DP, ou até mais negativo. Se o valor for positivo ou maior que -1, a massa óssea é considerada normal, e se estiver entre -1 e -2,49 diz-se que há “osteopenia”. Se o valor corresponder a osteopenia, mas já existirem fraturas por fragilidade, é feito o diagnóstico de osteoporose.Embora esse critério tenha sido originalmente baseado em medidas feitas no quadril com absorciometria de raio-X dual (DEXA), ele foi estendido para avaliar outros locais do esqueleto, e usando outras tecnologias. Há dúvidas entre os especialistas se essa generalização fornece as mesmas informações diagnósticas e preditivas. A medição no quadril é melhor para prever o risco de fratura de quadril do que a medição em outros locais, assim como a medição na coluna lombar é melhor para prever o risco de esmagamento vertebral.
Do ponto de vista do diagnóstico e da avaliação de muitos sujeitos, a utilização de aparelhos mais simples, às vezes portáteis, que fornecem informações rápidas e de menor custo, como DEXA do antebraço distal ou do calcâneo, ou ultrassonografia do calcâneo , é aceitável. falanges ou calcâneo. No entanto, os especialistas concordam que uma “osteoporose” diagnosticada em um sítio periférico deve ser confirmada por uma medida em um sítio axial, por DEXA ou tomografia computadorizada quantitativa. Além disso, a densitometria periférica não é aceita como válida para monitorar a resposta óssea ao tratamento com drogas osteoativas.
O laboratório também pode fornecer dados que indiquem o turnover com os chamados “marcadores”: fosfatase alcalina total ou sua insoenzima sérica de origem óssea e osteocalcina dão uma ideia da taxa de formação de osso novo (atividade osteoblástica), enquanto a piridinolina urinária e a desoxipiridinolina, e os peptídeos de colágeno tipo I (CTX, NTX) medidos no soro ou na urina, dão uma idéia da taxa de reabsorção óssea (atividade osteoclástica). Esses marcadores não fazem o diagnóstico de osteoporose, mas indicam se a rotatividade é alta ou normal e podem direcionar melhor o tipo de distúrbio subjacente; portanto, auxiliam na escolha do tratamento. Além disso, como variam de acordo com a variação da peça,Eles permitem avaliar a resposta ao tratamento em períodos mais curtos (semanas ou meses) do que os necessários para medir as alterações da massa óssea (mínimo 1 ano). Em idosos, e principalmente em institucionalizados que não vivam ao ar livre nem se exponham ao sol, a determinação do calcidiol (25-hidroxivitamina D) no soro e, se o valor for baixo, o do PTH sérico é extremamente útil. , uma vez que o hiperparatireoidismo secundário é uma causa comum de osteoporose senil e sua prevalência é alta em idosos.
Em suma, diante de um paciente com síndrome osteoporótica, os esforços do médico devem ser direcionados para a exclusão das causas corrigíveis (desnutrição, hipertireoidismo, hiperparatireoidismo, etc.).
Em todo paciente com mais de 50 anos que sofre uma fratura, a massa óssea deve ser avaliada com métodos objetivos e, a seguir, medidas preventivas ou curativas. A densidade óssea também deve ser medida em pessoas com dois ou mais dos fatores de risco listados na Tabela 2.
|
Tabela 2. Fatores de risco para osteoporose
|