por Juan Carlos Dupont
La palidez es el hallazgo físico más común asociado a la anemia, aunque su utilidad en el reconocimiento de la misma se ve limitada por una serie de factores que alteran la coloración de la piel. Las características raciales, el grosor y textura de la piel y las condiciones circulatorias momentáneas influyen sobre el color. Más aún, enfermedades adquiridas tales como la hemocromatosis, la enfermedad de Addison, la ictericia o ciertos efectos tóxicos de fármacos (por ejemplo, el busulfán) también pueden interferir en la posibilidad de detectar la palidez anémica. Sin embargo, aun en individuos muy pigmentados la presencia de anemia puede ser investigada en las palmas, las mucosas, los lechos ungueales y las conjuntivas palpebrales.
Existen dos determinantes importantes en el desarrollo de la palidez. Uno es la disminución de la concentración de hemoglobina y el segundo es la condición hemodinámica de la piel. Cuando el flujo sanguíneo se redistribuye hacia órganos vitales durante una hemorragia aguda, la intensidad de la palidez cutánea aumenta.
Anemia. El término "anemia" se utiliza comúnmente para referirse a una reducción de la concentración de hemoglobina o glóbulos rojos por debajo de los valores considerados normales para la población de referencia (tabla 17-1). Una disminución superior al 10% del valor medio se considera diagnóstica. Debe recordarse también que los valores medios normales dependen de la edad, del tipo de población y de la altura sobre el nivel del mar (tabla 17-1). Es importante tener en cuenta que los valores de referencia pueden incluir un 20-30% de población carenciada en hierro, como lo señalan algunos autores y la Organización Mundial de la Salud.
Anemia “espúrea”. Normalmente, la reducción de la concentración de glóbulos rojos refleja la reducción en la masa total de los mismos. Alteraciones del equilibrio hidroelectrolítico que condicionen un aumento del volumen plasmático, como sucede en el tercer trimestre del embarazo o secundarias a la sobrehidratación en la insuficiencia renal oligúrica y en la insuficiencia cardíaca congestiva, pueden ser consideradas erróneamente como estados anémicos, cuando en realidad sólo hay hemodilución. Como contrapartida, la disminución del volumen plasmático por diversos motivos puede llevar a una subvaloración de una anemia. Las situaciones clínicas que con más frecuencia pueden enmascarar una anemia por este mecanismo son: la diarrea infantil intensa y en los adultos la acidosis diabética y la obstrucción intestinal (tabla 17-2).
Síntomas y signos de la anemia
Los síntomas de la anemia dependen de la velocidad de su instalación y de la capacidad de ajuste cardiorrespiratorio del sujeto. Además, si preexiste una enfermedad vascular localizada asintomática, el desarrollo de anemia puede manifestarse por angina de pecho, claudicación intermitente o isquemia cerebral transitoria.
Lo común para individuos con anemia leve es que estén asintomáticos. En oportunidades, el ejercicio les produce disnea y palpitaciones. Los pacientes con anemia severa tienen síntomas aún en reposo y son regularmente incapaces de tolerar un esfuerzo físico.
En los individuos adultos, una disminución de la hemoglobina por debajo de 8 g por 100 mi les provoca un estado hiperdinámico que se manifiesta por taquicardia, pulso amplio, en oportunidades soplo sistólico eyectivo en los focos de la base, y en aquellos en que la reserva miocárdica está disminuida, se desarrolla insuficiencia cardíaca.
Otros síntomas atribuibles a trastornos circulatorios son cefaleas, vértigos, zumbido y eventualmente perdida del conocimiento. Algunos pacientes refieren insomnio e irritabilidad. Los síntomas gastrointestinales como anorexia, dispepsia o náuseas son consecuencia de la disminución del flujo esplácnico. En la esfera sexual la manifestación más común en el hombre es la disminución de la libido y en las mujeres amenorrea o hipermenorrea.
| Tabla 17-1. Valores medios sanguíneos normales a diferentes alturas sobre el nivel del mar. (Antioguía, Colombia) | ||||
| Altura (m) | Grupos | Eritrocitos x 106/mm3 |
Hemoglobina gramos % |
Hematócrito % |
| 50 | Niños | 4,45 | 13,0 | 40,9 |
| Mujeres | 4,32 | 13,1 | 41,5 | |
| Hombres | 5,03 | 15,5 | 47,9 | |
| 750 | Niños | 4,65 | 14,2 | 44,2 |
| Mujeres | 4,40 | 13,4 | 42,0 | |
| Hombres | 5,11 | 16,2 | 49,2 | |
| 1800 | Niños | 4,96 | 15,1 | 44,9 |
| Mujeres | 4,77 | 14,5 | 44,7 | |
| Hombres | 5,25 | 17,2 | 49,4 | |
| 2500 | Niños | 5,07 | 15,0 | 45,4 |
| Mujeres | 4,92 | 15,5 | 45,3 | |
| Hombres | 5,60 | 17,7 | 51,1 | |
| Tabla 17-2. Condiciones en las que hay una significativa desproporción entre el hematócrito y la masa globular total | ||
| Aumento del volumen plasmático | Disminución del volumen plasmático | Disminución del volumen plasmatico y de la masa globular |
|
|
|
Conceptos fisiológicos
Hemoglobina. En las formas más elementales de vida, el oxígeno viaja disuelto en los fluidos intersticiales. En especies más desarrolladas, como los moluscos, aparecen las metaloproteínas, que aumentan la capacidad de trasporte de oxígeno. Los animales superiores disponen de la hemoglobina, que es una proteína de un peso molecular de 64.500 con un grupo prostético denominado hem.
Una apropiada síntesis de hemoglobina involucra tres vías: a) metabolismo del hierro, b) biosíntesis del hem, y c) síntesis de la globina.
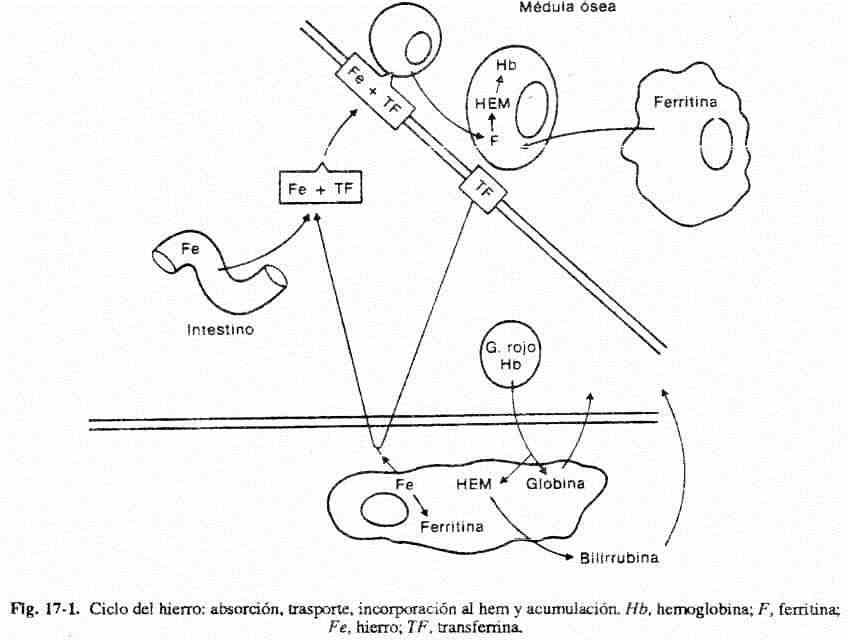
Metabolismo del hierro. La absorción de hierro en la porción proximal del yeyuno se realiza por lo menos de dos formas: a) como hierro unido al grupo hem, o b) como hierro reducido (Fe++). Inicialmente la acidez del jugo gástrico separa la porción globínica de las diferentes proteínas biológicas que contienen hierro, y el grupo hemina (hem + Fe+++) se absorbe intacto. El hierro contenido en otros alimentos en formas diferentes al hem 4 + Fe+++ debe ser reducido a Fe++ para que luego sea absorbido.
Cuando el hierro en forma de hem ingresa a la célula de la mucosa, el anillo porfírínico es olivado por la hemoxigenasa, y del mismo modo que el ion Fe++, permanece pocas horas en dicha célula. Luego pasa al plasma donde circula unido a la trasferrina, que es una glucoproteína trasportadora de hierro de 74.000 de peso molecular. En los sujetos normales la cantidad de hierro en el organismo permanece relativamente fija en 35 a 50 mg/kg de peso. El 0,1% circula en el plasma unido a la trasferrina, el 30% se encuentra en sus formas de almacenamiento (ferritína y hemosiderina), y el resto forma parte de la hemoglobina y la mioglobina. La necesidad diaria de hierro es de 1 mg, que es lo que se pierde por descamación epitelial del intestino. Esta necesidad se duplica en la mujer que menstrua y se triplica durante el embarazo. Los precursores del eritrocito maduro, desde el pronormoblasto hasta el reticulocito, incorporan hasta el 80% del hierro circulante en el plasma. Este proceso se efectúa en la médula ósea a través de receptores específicos de los eritroblastos para el complejo Fe-transferrina (fig 17-1).
Biosíntesis del hem. En la mitocondria, la succinil-coenzima A se une a la glicina reguladora por la sintetasa del ácido 3-aminolevulínico. Luego, fuera de la mitocondria, se efectúa la síntesis del anillo tetrapirrólico que, nuevamente en la cresta mitocondrial y ya convertido en protoporfirina 9, se une al hierro por intermedio de la enzima hem-sintetasa para luego pasar al citoplasma.
Síntesis de globina. Esta proteína es un tetrámero compuesto por dos pares de cadenas polipeptídicas designadas alfa, beta, gamma y delta, cada uno de los cuales está unido en forma covalente con el grupo hem. La síntesis de la globina se produce en el proeritroblasto. Cada una de las cadenas es regulada por un gen heredado de cada uno de los padres.
En el citoplasma estos tetrámeros se unen al grupo prostético hem y forman la hemoglobina. El 97% de la Hb del adulto es HbA (Alfa2 Beta2) y el 3% es HbA2 (Alfa2 Delta2). En el feto existe la hemoglobina F (Alfa2 Gamma2), que en el último trimestre de gestación cambia a síntesis de cadenas Beta.
Función de la hemoglobina. Durante la circulación por el pulmón, la hemoglobina se satura casi totalmente con oxígeno (1,34 ml de O2 por gramo de Hb). En el lecho capilar el oxígeno es extraído por los tejidos. Este mecanismo se hace posible por el cambio de afinidad por el oxígeno a diferentes presiones parciales de oxígeno (curva sigmoide) (ver fig. 16-2). La afinidad por el oxígeno también es influida por el pH, la PCO2 y el 2,3-difosfoglicerato (2,3-DPG). Cada uno de estos factores, cuando aumentan, desplazan la curva hacia la derecha, aumentando la entrega de O2 por parte de la hemoglobina.
El 2,3-DPG se une a la cadena p de la desoxihemoglobina, disminuyendo aún más su afinidad por el oxígeno (ver fig 17-2).
Eritropoyesis. Los eritrocitos derivan de una célula madre pluripotente, que además da origen a las serles granulocítica, monocítica, megacariocíiica y linfocitaria.
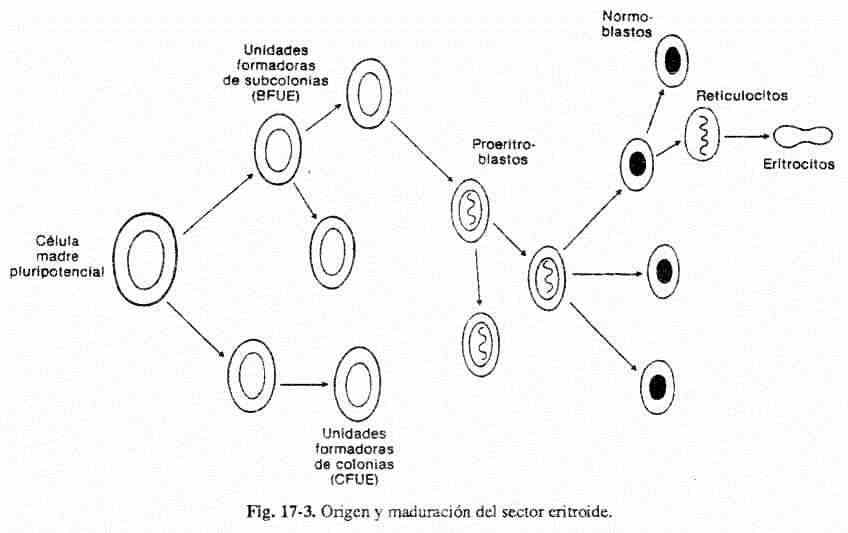
Se han reconocido por lo menos dos precursores de los eritrocitos en cultivos in vitro de sangre circulante. Las EBFU (erythroid burst forming units - unidades formadoras de subcolonias eritroides) aparecen tardíamente (10 a 15 días) en los cultivos y representan a estadios más tempranos de la evolución del eritrohlasto. Las ECFU (erythroid colony forming units - unidades formadoras de colonias eritroides) aparecen más tempranamente (4 a 7 días) en los cultivos, son sensibles a la eritropoyetina, y también son reguladas por subpoblaciones linfocitarias T.
La eritropoyetina es una proteína de 32.000 daltons que circula en el plasma como una apoenzima. Los riñones producen un factor activador de la eritropoyetina en condiciones de hipoxia. Una vez activada interactúa con los eritroblastos, a través de receptores, induciendo mitosis e incremento en la síntesis de hemoglobina. Completada esta última, el núcleo se expulsa del normoblasto y la célula pasa a la circulación corno reticulocito, perdiendo luego sus mitocondrias y ribosomas en 24 horas, y trasformándose así en eritrocito maduro (fig. 17-3).
Evaluación de un paciente con anemia
La evaluación del paciente con anemia (tabla 17-3) requiere, como en todas las disciplinas clínicas, un meticuloso interrogatorio y examen físico de modo que la orientación inicial ahorre pasos innecesarios en la investigación del origen de la misma. A continuación, se sintetizará esquemáticamente el estudio de un paciente anémico.
Después de establecer que un paciente presenta anemia, la primera pregunta a efectuarse es si corresponde a un déficit de producción o a un aumento de destrucción. Los reticulocitos, que son glóbulos rojos inmaduros, permiten dar esta respuesta. La reticulocitosis implica un grado de producción elevado y, por lo tanto, si existe anemia, ésta habrá sido causada por un mecanismo hemolítico o por una hemorragia aguda reciente. Existen otros motivos de incremento de reticulocitos en pacientes anémicos tales como la invasión medular por tumores o granulomas (mieloptisis) y la inyección reciente de vitamina B12 en pacientes con anemia perniciosa. El modo más apropiado de determinar la tasa de producción de eritrocitos es:
Indice reticulocitario = % de reticulocitos x (hematócrito del paciente / hematócrito normal)
Si el índice es superior a 1 se lo considera hiperregenerativo y si es inferior a 1 hiporregenerativo. Cuando la médula está muy estimulada y hay eritroblastos en sangre periférica, este índice debe ser dividido por dos.
Examen del frotis de sangre. La importancia del extendido reside en la facilidad con que se lo obtiene y en la información que brinda sobre el tamaño, la coloración y las alteraciones de la forma; asimismo, permite detectar la existencia de inclusiones.
Se denomina anisocitosis a la presencia de eritrocitos de diferente tamaño: a) normocitos, que varían entre 7,2 y 7,9 micrones; b) macrocitos, que son hematíes con un tamaño generalmente superior a los 9 micrones; pueden corresponder a hematíes jóvenes (reticulocitos) o a megalocitos de la anemia megaloblásüca, y c) microcitos, en los cuales el diámetro es inferior a los 6 micrones. Se los observa en trastornos de la síntesis de hemoglobina (ferropenia, talasemia, anemia sideroblástica).
Se llama anisocromía a la distribución irregular del contenido de hemoglobina en diferentes eritrocitos: a) los normocrómicos tienen contenido normal de Hb y la palidez central no ocupa más de un tercio de su diámetro, y b) en los hipocrómicos existe una disminución global de la coloración y aumento de la palidez central. Regularmente son microcitos y su aparición responde a las mismas causas.
La poiquilocitosis es el término que define la presencia de hematíes de distinta forma: a) en los esferocitos la forma normal bicóncava ha sido reemplazada por la forma esférica, con lo que se reducen los diámetros (6 micrones) pero no el volumen; dan la impresión falsa de ser hipercrómicos; b) los eliptocitos son de forma oval o elíptica; c) los dianocitos (target cells) se producen por disminución del contenido de hemoglobina o por aumento de la relación superficie/volumen en ciertas hepatopatías (déficit de lecitin-coiesterol-acil-transferasa); lo que se observa es una distribución atípica de la hemoglobina, con el centro teñido remedando un blanco de tiro; d) los drepanocitos son hematíes en forma de media luna, alargada, y se producen en presencia de hemoglobina S; e) los esquistocitos son fragmentos de eritrocitos de forma irregular, pequeños y con dos o tres puntas que regularmente aparecen cuando hay lesiones capilares (síndrome urémico-hemolítico, coagulación intravascular diseminada) o prótesis valvulares cardíacas; f) los dacriocitos son hematíes en gota característicos de las mielofibrosis, aunque también pueden verse en algunos estados hemolíticos (Hb H, talasemia).
En líneas generales, para que alguna de las alteraciones tenga jerarquía en cuanto a la orientación diagnóstica, tiene que estar presente en más del 10 al 30% de los eritrocitos.
Inclusiones intracitoplasmátícas. En el punteado basófilo se trata de granulaciones de color azul grisáceo que representan a los ribosomas y mitocondrias precipitadas por la coloración. Regularmente se observan en los trastornos de la síntesis de hemoglobina.
Los cuerpos de Howell-Jolly son esféricos y corresponden a restos nucleares. Normalmente son extraídos de los eritrocitos en el bazo, y por lo tanto son expresión de asplenia.
Los anillos de Cabot son formaciones filiformes violáceas, circulares o plegadas en ocho, y se los observa en los trastornos diseritropoyéticos primarios o secundarios (leucemias, mielofibrosis).
Examen microscópico de la médula ósea. Se lo indica cuando el mecanismo de la anemia no puede ser explicado con los elementos clínicos disponibles. La mayoría de las muestras pueden ser obtenidas por punción de la cresta ilíaca posterosuperior, que provoca menos molestias que la punción esternal. El medulograma en las anemias proporciona información sobre: a) la celularidad total y eritroide; b) la relación mieloeritroide; c) la calidad de la eritropoyesis; d) la presencia de células extrañas a la médula ósea (tumores, granuloma), y e)la existencia de depósitos de hemosiderina (tinción de Perls).
Se pueden identificar cuatro tipos principales de trastornos de la eritropoyesis:
a) Sideropénica. Existe moderada hiperplasia eritroide, frecuentemente con detención de la maduración a nivel de eritroblastos basófilos y eritroblastos pequeños con citoplasma escaso y en oportunidades con bordes desflecados. Si se efectúa una tinción de Perls, los depósitos de hemosiderina y los sideroblastos son negativos. En los trastornos crónicos los sideroblastos son negativos, pero los depósitos de hemosiderina son elevados.
b) Sideroblástica. Se observan sideroblastos patológicos (depósitos en anillo) y hemosiderina muy aumentada.
c) Megaloblástica. Por déficit de ácido fólico o de vitamina B12 se producen alteraciones de la maduración nuclear, lo cual se manifiesta por hiperplasia eritroide con eritroblastos gigantes (megaloblastos), fragmentación nuclear, mitosis, y remanentes nucleares en los eritroblastos más maduros.
d) Displástica. Generalmente existe una hiperplasia del sector eritroide, con alteraciones del tamaño, la forma y la cantidad de núcleos (bi, tri, tetranucleados), que pueden estar acompañados de cambios megaloblásticos y de eritroblastos en anillo. Estas alteraciones son frecuentes en las anemias refractarias y en los síndromes preleucémicos.
Indices hematimétricos. Con el advenimiento de los contadores electrónicos (tipo Coulter), los índices de volumen y de concentración hemoglobínica corpusculares se han tomado mucho más precisos que con métodos manuales. Los contadores hacen una medición directa de los eritrocitos (GR/microlitros) y del volumen corpuscular medio (VCM)