por Dr. Facundo Daminato
Oliguria
Se denomina oliguria a un volumen urinario insuficiente para eliminar los desechos tóxicos del organismo, por lo general inferior a 400 ml diarios en un adulto de 70 Kg de peso.
Anuria
Ausencia de flujo urinario, causada principalmente por obstrucción de la vía urinaria o por obstrucción en el árbol arterial o venoso renal. Existen enfermedades parenquimatosas que pueden también provocar ausencia de flujo urinario, tales como la necrosis cortical o la Glomerulonefritis rápidamente progresiva pero en mucha menor frecuencia que las causas anteriores por lo que deben descartarse las causas obstructivas antes de pensar en otra etiología.
Uremia
Las concentraciones plasmáticas de urea y creatinina se miden para valorar el filtrado glomerular. Ambas sustancias son producidas constantemente en el hígado y músculos respectivamente. Estas sustancias, sufren una filtración glomerular completa y no son reabsorbidos en gran cantidad por los túbulos renales, por lo que su aclaramiento tiende a ser un reflejo del filtrado glomerular. Cuando éste cae, se produce un incremento en sus concentraciones séricas dando lugar al estado de uremia o hiperazoemia. La creatinina es un índice más fiable del filtrado glomerular que la urea, debido a la menor retrodifusión de esta última desde la luz tubular a la sangre peritubular. El filtrado glomerular puede estar reducido por una disminución de la filtración de nefronas funcionantes individuales o por una reducción en el número de las mismas.
FILTRADO GLOMERULAR REDUCIDO EN CADA NEFRONA
Cuando se produce un descenso en el volumen extracelular, se genera una respuesta importante en el riñón normal que se caracteriza por una reducción de la filtración glomerular de cada nefrona y la reabsorción subsiguiente de cloruro de sodio (ClNa) y agua que llega a los túbulos. La hiperazoemia resultante se denomina prerrenal, y en ella la concentración urinaria de Na desciende por debajo de los 20 meq/l. La secreción de vasopresina (ADH) está estimulada por la reducción del volumen del volumen de líquido extracelular y, en consecuencia, los túbulos distales y los conductos colectores se hacen totalmente permeables al agua. Los mecanismos concentradores de la médula renal son muy eficaces cuando el flujo a través de las asas de Henle y los conductos colectores es bajo. Como consecuencia, el filtrado que escapa a la reabsorción en el túbulo proximal sufre una concentración osmótica máxima, el volumen urinario es pequeño y posee una elevada osmolaridad, superior a 500 mosmoles por Kg de agua. La mayor parte de la creatinina filtrada escapa a la reabsorción tubular, y en consecuencia la proporción entre las concentraciones de creatinina urinaria y plasmática (U/P) es muy alta, de 40 o superior. Dado que la urea difunde de forma retrógrada más que la creatinina, las cifras de nitrógeno ureico sanguíneo (BUN) se elevan más que las de creatinina sérica. Normalmente la proporción entre BUN y creatinina sérica es 10:1; con la reducción de volumen extracelular esta proporción aumenta. Existen otras situaciones donde esta relación puede alterarse tales como el tratamiento con tetraciclinas, el tratamiento con corticoides, presencia de sangre en el tubo digestivo alto y el aumento del metabolismo de las proteínas debido a traumatismos o quemaduras.
Cuadro 1. Mecanismos fisiopatológicos de hiperazoemia prerrenal
| Mecanismos de reducción del FG | Ejemplos clínicos | Oliguria | Osm en orina | NaU | BUN Cr sérica |
| Túbulos normales (Hiperazoemia prerrenal) |
|
Casi siempre | > 500 | < 20 | > 10 |
| Túbulos lesionados (Insuficiencia renal aguda) |
|
Frecuente | < 350 | > 40 | 10 |
Puede aparecer hiperazoemia prerrenal en cualquier proceso formador de edema durante la fase de retención de ClNa y agua. Son ejemplos típicos el síndrome nefrótico y la cirrosis hepática con ascitis. Cuando se administra en estos casos algún diurético, el volumen y la concentración urinaria de Na pueden ser normales, pero al retirarlos se vuelven a activar los mecanismos de retención de Na y agua, dando lugar nuevamente a un estado de oliguria. También puede verse hiperazoemia prerrenal cuando el flujo sanguíneo renal está reducido debido a hipotensión sistémica, oclusión incompleta de arteria o vena renal, u otra causa.
Ciertas enfermedades renales agudas que producen hiperazoemia disminuyen la función glomerular de cada nefrona y al mismo tiempo lesionan los túbulos lo suficiente como para reducir e incluso abolir su función reabsortiva, produciendo una IRA. La necrosis tubular aguda (NTA), los agentes nefrotóxicos y la enfermedad tubulointersticial aguda constituyen excelentes ejemplos. Aparecen hiperazoemia y oliguria pero la concentración urinaria de Na supera los 20 meq/l y habitualmente los 40 meq/l.
REDUCCION DEL NÚMERO DE NEFRONAS
Según la función de cada nefrona podemos ver tres tipos de situaciones:
a) Filtración glomerular de cada nefrona aumentada
Si se extirpa un riñón, el otro experimenta un aumento de tamaño a expensas de un aumento de tamaño de sus nefronas (hipertrofia) y de esta manera, aumenta la filtración glomerular aproximándose al FG normal aportado por dos riñones. Los túbulos están sobreperfundidos con filtrado, pero soportan la carga reabsortiva. Si se extirpan más nefronas del riñón único, las nefronas remanentes aumentan aún más el tamaño y por ende el FG. En este caso, aparece hiperazoemia debido a que a pesar de aumentar el tamaño las nefronas remanentes, el FG global es bajo. La conservación de agua y Na son menores por lo que se debe asegurar una ingesta mayor. Los estado clínicos que producen este cuadro son la pérdida quirúrgica de parénquima renal secundaria a traumatismos, neoplasias, litiasis y destrucción del parénquima por infecciones bacterianas o tuberculosis, enfermedad poliquística y quística medular renales y todas las nefropatías tubulointersticiales crónicas.
b) Filtración glomerular de Cada nefrona normal
No parece la función glomerular de cada nefrona aumente a pesar de la reducción en el número de nefronas en enfermedades tales como la Glomerulonefritis y la glomeruloesclerosis DBT, en las que el glomérulo es el sitio principal de la lesión. En estas enfermedades el FG total disminuye en relación directa con el número de nefronas y no se mantiene mediante una elevación de la función glomerular en cada nefrona
La conservación de sodio y agua está conservada por el escaso daño tubular. Puede observarse oliguria con baja concentración de sodio urinario. La proporción de urea/creatinina se eleva notablemente.
c) Filtración glomerular de cada nefrona reducida
En los pacientes con nefropatía crónica en los cuales el FG total ha sido suficiente para el mantenimiento de la vida tan solo a expensas de una filtración glomerular en cada nefrona aumentada, la deshidratación inadvertida o cualquier otro factor que disminuya el filtrado por cada nefrona puede provocar oliguria e hiperazoemia intensa.
Cuadro 2: Reducción del número de nefronas
| Causa | Presencia de oliguria | Osmolaridad urinaria | Sodio urinario | Bun/Cr P | |
| FG en cada nefrona elevada | Nefritis tubulointersticial, pérdida de tejido renal | rara | 290 | > 40 | 10 |
| FG en cada nefrona normal | GNF crónica, Nefropatía DBT | rara | 100-350 | >< 10 | > 10 |
| FG en cada nefrona reducida | Cualquiera de los anteriores | frecuente | 290 | > 20 | > 10 |
DIAGNOSTICO DE HIPERAZOEMIA
La constatación de concentración elevada de productos nitrogenados y/o disminución de la diuresis obliga al médico a iniciar un proceso deductivo que le permita discernir el tipo de insuficiencia renal ante la que se encuentra y si es posible, la noxa que la produce. Para ello, recurrirá a un proceso escalonado de exclusión basado en la realización de una historia clínica exhaustiva, que incluya una anamnesis cuidadosa de los antecedentes personales del enfermo, una exploración meticulosa y la utilización ponderada y secuencial de pruebas complementarias.

Mientras que el diagnóstico sindrómico de enfermedad renal es relativamente sencillo, el diagnóstico etiológico del que depende el tratamiento eficaz del paciente es muchas veces difícil. Por ello, aconsejamos analizar las siguientes reflexiones:
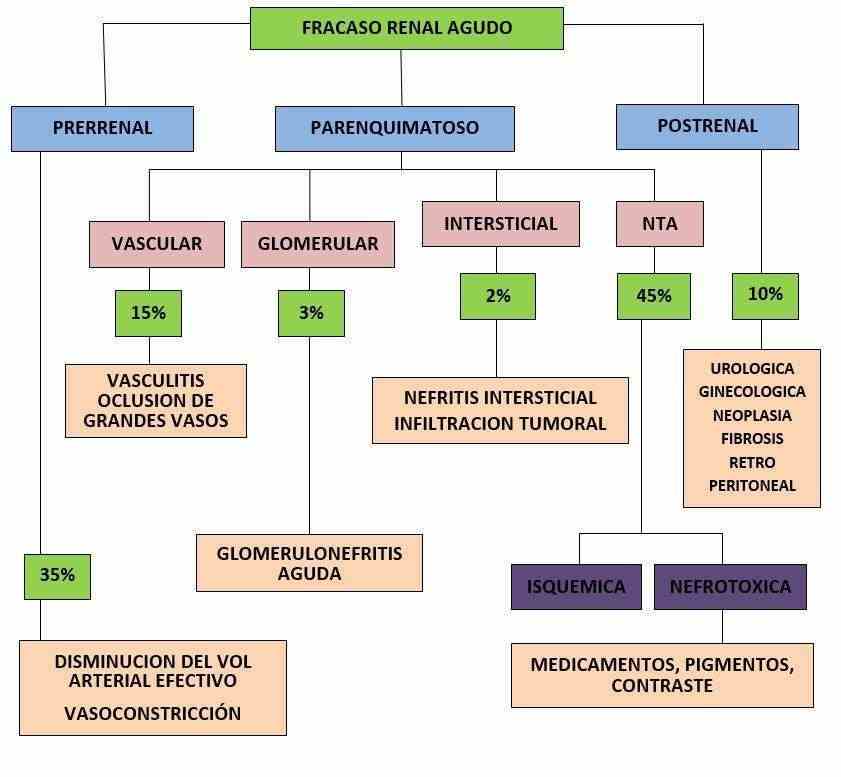
a) Recordar que las causas que pueden ocasionar un fracaso renal son muy diversas. La alteración o el daño de cualquiera de las estructuras renales (vasos intrarrenales, glomérulos, túbulos e intersticio) puede producir IR parenquimatosa. Asimismo, factores ajenos al propio riñón pero que alteren su hemodinámica (factores prerrenales) o impidan la eliminación de orina (factores postrenales) pueden causarlo.
b) Saber que el fracaso renal en el hombre es muchas veces multifactorial. Por ejemplo, la reducción de volumen, el bajo gasto y la nefrotoxicidad pueden ser causas coexistentes en una necrosis tubular aguda (NTA).
c) Conocer que el fracaso renal agudo, es un proceso dinámico que puede evolucionar a estadíos más graves. Así, una falla prerrenal puede evolucionar a parenquimatosa si la injuria se mantiene y provocar una NTA.
d) Ser consciente de que nunca hay que recurrir a una "tormenta" diagnóstica, realizando múltiples análisis y exploraciones complementarias, sino que los procedimientos diagnósticos deben escalonarse, en función a su eficacia e inocuidad para el enfermo.
IRC VS IRA. SIGNOS Y SINTOMAS
En ocasiones, la distinción entre estas situaciones es difícil. El primer punto a investigar es la posible existencia de controles analíticos previos de la función renal obtenidos en reconocimientos rutinarios o en procesos patológicos anteriores, que permitirán conocer si el deterioro actual es agudo o crónico. La existencia de antecedentes de una enfermedad renal anterior sugerirá una evolución del proceso hacia la IRC. Hay que tener en cuenta también que un enfermo con IRC puede tener un deterioro agudo de origen similar al de un sujeto sano, o bien debido a un brote de su enfermedad de base. Los controles analíticos después de detectar una elevación de los productos nitrogenados son muy orientativos: en la IRC, los valores permanecen constantes, mientras que en la IRA se aprecian incrementos diarios a menudo de más de 0,5 mg/dl en la creatinina plasmática. En caso de no tener datos previos de la función renal, la sintomatología del paciente es muy útil. El síndrome urémico, caracterizado por astenia, anorexia, somnolencia, calambres, nauseas o vómitos matutinos, poliuria o polidipsia de larga evolución indican un proceso crónico, raros de ver en la IRA. También es posible encontrar el tinte ureocromo de la piel, que debe diferenciarse de la ictericia, también presente en un proceso de larga evolución. La presencia de anemia bien tolerada, hipocalcemia e hiperfosfatemia o de acidosis metabólica también nos encamina a pensar en un proceso crónico (pero también puede verse en un proceso agudo de un poco más de tiempo de evolución). Con respecto a métodos complementarios tales como la ecografía renal, la presencia de riñones disminuidos de tamaño nos habla de un proceso netamente crónico.
PRUEBAS COMPLEMENTARIAS
Las determinaciones en sangre y orina de sodio, potasio, osmolalidad, urea y creatinina, con los que se pueden establecer diferentes índices diagnósticos, constituye una ayuda importante en el diagnóstico de hiperazoemia. La excreción fraccional de sodio: EFNa = (NaU x CrP / NaP x CrU) x100 el que tiene mayor sensibilidad y especificidad para diagnosticar el tipo de fracaso renal agudo. En general valores inferiores a 1 sugieren un origen prerrenal,mientras que los superiores a 2 se verían en las NTA. En ocasiones, valores intermedios de EFNa entre 1 y 3 pueden verse en cuadros donde una cantidad de nefronas están en estadio prerrenal y responde a la expansión con líquidos y otras presentan NTA, las cuales mantienen elevadas las cifras de urea y creatinina. Con el uso de diuréticos esta determinación pierde valor por lo que se utiliza la excreción fraccional de urea que valores por debajo del 35% indican una causa prerrenal y por encima, daño parenquimatoso.
Otro examen de mucho valor en la práctica diaria es el sedimento urinario. En las NTA suele mostrar solo cilindruria granulosa y/o hialina de coloración parduzca, debido a detritus celulares del epitelio tubular y la presencia de proteína de Tamm-Horsfall, células tubulares descamadas. En la IR prerrenal el sedimento es normal. En presencia de hematuria dismórfica, cilindruria, leucocituria, estamos frente a una IR de etiología parenquimatosa. Es preciso utilizar la tinción de Wright para diagnosticar eosinofiluria si sospechamos una nefritis tubulointersticial. La observación de cristales de oxalato de calcio se ve en intoxicaciones por etilenglicol, metotrexato o metoxiflurano. Los de ácido úrico en la lisis tumoral.
OTROS METODOS COMPLEMENTARIOS
Ecografía: El tamaño renal normal (10-12 cm) está disminuido en la ERC, excepto en poliquistosis, mieloma, amiloidosis y DBT en estadios no terminales.
En los procesos agudos parenquimatosos es posible observar aumento de la ecogenicidad pero es inespecífico. Pueden verse riñones grandes debido al edema del intersticio renal (NTIA, linfoma, vasculitis y GNF).
Puede verse aumento de tamaño renal en procesos obstructivos donde veríamos dilatación pielocalicial. Cuando la obstrucción se produjo en las últimas 24 a 48 hs puede no verse dilatación todavía, por lo que debe repetirse el estudio. En este caso, un espesor corticomedular conservado (2 cm) habla de una obstrucción aguda.
Ecografía doppler: evalúa la vasculatura renal y descarta patología a nivel de grandes y medianos vasos (estenosis, dilataciones, embolias, etc).
Radiografía simple de abdomen: Proporciona información sobre la morfología renal, presencia de litiasis y calcificaciones vasculares.
Tomografía axial computada: Útil para cuadros obstructivos y sus causas. Pielonefritis.
Estudios isotópicos: De escasa utilidad en el fracaso renal.
Biopsia renal: Solamente es útil en sospecha de fracaso renal por glomerulopatía, o cuando la IR perdura a pesar del tratamiento instaurado de acuerdo al diagnóstico de sospecha inicial.